Feladat:
Az előzőekben hidrogén-peroxiddal végeztük a luminol oxidációját Cu(II)-ion katalizátor jelenlétében, ennél egy sokkal egyszerűbben megvalósított oxidációt hajtunk végre nátrium-hipoklorit oldattal. Ez egy sokkal gyorsabb oxidáció, ezért erősebb kemilumineszcenciát észlelhetünk, viszont a kemilumineszcencia időtartama jelentősen lecsökken.
Készítsünk 2 oldatot:
– 1-2 pasztilla, vagy 0,3-0,5g Nátrium-hidroxid (NaOH), vagy kálium-hidroxid (KOH) granulátumot feloldunk 200-300ml desztillált vízben (vagy csapvízben), majd késhegynyi (kb.0.1g) luminolt beleadagolunk, rázogatással feloldjuk.
– 20ml háztartási Hypo-t 1:1 arányban meghígítunk d-vízzel (vagy csapvízzel).
Besötétítés után a két oldatot összeöntjük, kék kemilumineszcenciát tapasztalunk.
Nézzük meg és hasonlítsuk össze a luminol oxidációja hidrogén-peroxid oldattal c. kísérlettel!
Figyelmeztető jelölések
A kísérlet végzése közben védőkesztyű használata kötelező! A kísérlet végzése közben védőszemüveg használata kötelező!
Videó
| → | 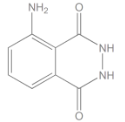 Luminol szerkezeti képlete Luminol szerkezeti képlete |
Magyarázat
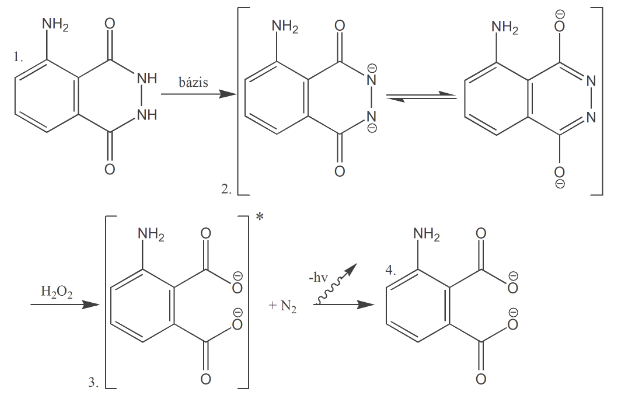
A luminol lúgos közegben dianionná alakul, ezt a formát könnyen oxidálhatjuk nátrium-hipoklorittal vagy hidrogén-peroxiddal (A Cu2+ katalizálja a H2O2 bomlását). Az oxidáció következtében aminoftalát-ion képződik nitrogénfelszabadulás közben. Az aminoftalát-ion energetikailag gerjesztett állapotban van, foton kisugárzása közben azonban alapállapotba kerül. A kisugárzott fényt kéknek látjuk a hullámhossza 424nm.
Az oxidáció mechanizmusa