Feladat
Szilárd nátrium-szulfitra sósavat csepegtetünk, és a folyamatban fejlődő gáz egy részét Lugol-oldatba, másik részét kén-hidrogénes vízbe vezetjük. Írja le és magyarázza meg a várható tapasztalatokat, és adja meg a végbemenő folyamatok reakcióegyenletét!
Videó
 |
Megfigyelések, tapasztalatok, következtetések
Kén-dioxid gázt legegyszerűbben nátrium-szulfit és sósav reakciójával tudunk előállítani: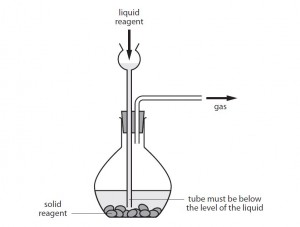
Na2SO3 + 2 HCl → SO2 + 2 NaCl + H2O
Kénhidrogénes vizet a vas-szulfidból sósavval felszabadított kén-hidrogén vízbe vezetésével nyerjük:
FeS + 2 HCl → FeCl2 + H2S
Előállításukhoz a jobb oldalon látható készüléket használhatjuk például. A solid reagent ebben az esetben a nátrium-szulfit vagy a vas-szulfid. A liquid reagent a sósav. A távozó gáz a SO2 vagy a H2S.
A videóban a jobb oldali kémcsőben kénhidrogénes víz volt amibe előzőleg kén-dioxid gázt vezettünk, sajnos azt a részt nem vettem fel. A kivált finom porszerű elemi kén sárgás fehéres színe látható.
SO2 + 2 H2S = 3 S + 2 H2O
A baloldali kémcsőben Lugol-oldat (Kálium-jodidos jód oldat) volt, amibe SO2 gázt vezettük, néhány másodperc alatt az oldat elszíntelenedett. Az elemi jód jodid-ionná redukálódott, ami színtelen. A kén-dioxid vízzel reagálva kénessavat alkot, a kénessavat a jód kénsavvá oxidálja. Különböző spektroszkópiás módszerekkel vizsgálva a kén-dioxid vizes oldatát a szulfit-ionok jelenlétét nem lehetett kimutatni, a hidrogén-szulfit ionok azonban képződnek.
első lépésben hidrogén-szulfit SO2 + 2 H2O = HSO3– + H3O+
második lépésben szulfit képződikHSO3– + H2O = SO32- + H3O+
A redox reakció egyenlete pedig:
HSO3– + I2 + H2O = SO42- + 2 I– + 3 H+
