Luminol oxidációja nátrium-hipoklorit oldattal
A luminol lúgos közegben dianionná alakul, ezt a formát könnyen oxidálhatjuk nátrium-hipoklorittal vagy hidrogén-peroxiddal (A Cu2+ katalizálja a H2O2 bomlását). Az oxidáció következtében aminoftalát-ion képződik nitrogénfelszabadulás közben. Az aminoftalát-ion energetikailag gerjesztett állapotban van, foton kisugárzása közben azonban alapállapotba kerül. A kisugárzott fényt kéknek látjuk a hullámhossza 424nm.
Érdekes kémiai kísérletek
Mindenféle érdekes kémiai kísérleteket találhatsz itt.
Nitrozil-vas(II)-szulfát előállítása
Nitrozil-vas(II)-szulfát előállítása
1 cm3 reagens kálium-nitrát oldathoz adjunk kis részletekben 3 cm3 cc.H2SO4-oldatot, a kémcsövet közben hűtsük csapvízzel (forró oldatban a [nitrozil-vas(II)] komplex elbomlik). A szobahőmérsékletű oldat tetejére óvatosan rétegezzünk frissen készített vas(II)-szulfát oldatot, a jellegzetes barna gyűrű hamar megjelenik.
Read MoreKróm(VI)-oxid-peroxid vagy peroxo-krómsav előállítása
Króm(VI)-oxid-peroxid vagy peroxo-krómsav előállítása
Peroxo-krómsav Cr(O2)2O egy instabil vegyület, mint a peroxidok általában. Könnyen előállítható, ha hidrogén- peroxid savval (pl. kénsavval) megsavanyított oldatához kálium-kromátot, dikromátot adunk, de akkor is keletkezik ha pl. kromil-kloridot savas hidrogén-peroxid oldatba vezetünk.
Read MoreCsersavak kimutatása növényi levelekből
Csersavak kimutatása növényi levelekből
A tanninok, más néven csersavak, keserű ízű, növényi eredetű polifenolok, amelyek összekötik és kicsapják a fehérjéket. A szövetes növények tannoszóma nevű sejtszervecskéjében termelődnek. A “tannin” mint kifejezés használatos minden sok hidroxilcsoportot és karboxilcsoportot tartalmazó polifenolos vegyületre amelyek más makromolekulákkal komplex képzésre képesek. Tanninok molekulasúlya 500-tól több mint 3000-ig terjed, ezeket galluszsav -észterek alkotják, akár 20.000 is lehet, ezek a proantocianidinek.
Read MoreDiana fája
Diana fája
Kémcsőben lévő higanycseppre ezüst-nitrát oldatot öntünk, a higany felületén azonnal megindul a fémes ezüst kiválása, mely kb. fél óra múlva 1-2 centiméteres ezüst-fává növi ki magát. A képződött ezüst amalgámot képez a higannyal, amely érintkezik az ezüst-ionokkal, melyeket redukál, így azok rárakódnak az amalgám felületére, faszerű szerkezetet hozva ezzel létre.
A reakció során a higany oldatba megy higany(I)-nitrát formájában, az ezüst-ionok fémezüstté redukálódnak.
Ha meg akarunk bizonyosodni, hogy az oldat Higany(I)-ionokat tartalmaz, pipettával mintát veszünk a kémcsőből, és tömény ammónia-oldatot adunk hozzá, fekete csapadék keletkezik. A higany(II)-ionok fehér csapadékot képeznek az ammónia oldattal.
Vanádium oxidációs állapotai
Vanádium oxidációs állapotai
Ammónium-metavanadátból kiindulva a vanádium különböző oxidációs állapotú ionjait fogjuk előállítani.
Ezüst-[tetrajodo-merkurát(II)] előállítása
Ezüst-[tetrajodo-merkurát(II)] előállítása
Ezüst-[tetrajodo-merkurát(II)] termokolor festék előállítása és színváltozásának vizsgálata.
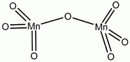
Mangán-heptoxid képződése és oxidáló tulajdonsága
Mangán-heptoxid képződése és oxidáló tulajdonsága
Finoman elporított néhány tized gramm kálium-permanganátot porcelántálban kevés tömény kénsavval keverjük össze, majd ebbe a keverékbe kis vattacsomót dobunk (biztonságosabb, ha a keverékbe üvegbotot mártunk, és ezzel érintünk meg egy vattacsomót). A kénsav hatására mangán(VII)-oxid keletkezik ami a vattát olyan hevesen oxidálja, hogy az lángra lobban. A kísérletet fülkében óvatosan hajtsuk végre. Nagyobb mennyiségű KMnO4-ra tömény kénsavat öntve, a reakcióelegy felmelegedése miatt a Mn2O7 robbanásszerűen bomlik.
Read MorePiroforos vas(II)-oxid előállítása, és égése
Piroforos vas(II)-oxid előállítása, és égése
Read MoreNéhány szervetlen kémiás rekcióegyenlet
Szervetlen kémiás rekcióegyenletek
Read More






![Ezüst-[tetrajodo-merkurát(II)] előállítása Ezüst-[tetrajodo-merkurát(II)] előállítása](http://weblaboratorium.hu/wp-content/uploads/2015/10/K2HgI4-200x140.png)